神経興奮を制御するためには、カリウムチャネル(KCNQ2/3)が活動電位の開始場所である軸索起始部(AIS)へ適切に「局在」し、かつ正常に「機能」することが求められます。KCNQ2/3が働かないと神経が過剰に興奮し、てんかんなど多くの神経・精神疾患の原因となります。これまで、KCNQ2/3のAIS局在は足場タンパク質(アンキリンG)との結合により制御される一方、そのチャネル機能は膜電位の感知に伴う一連の構造変化により制御されることが知られていました。しかし、これら2つの制御機構は長らく独立した別物とみなされ、両者の関連性は不明でした。
今回我々は、てんかん関連変異を含む多様な機能不全KCNQ2/3変異体の解析により、KCNQ2/3の機能性が低いほど、AISへの局在効率も低くなるという因果関係を発見しました(図1)。さらに、1分子イメージング技術を組み合わせることで、KCNQ2/3が活性化構造をとるとアンキリンGへの結合が強まり、AISに安定して配置されるという分子機構を解明しました。逆に、てんかんに関連する遺伝子変異によって機能性が低下したKCNQ2/3はアンキリンGと十分に結合できず、AISから排除されます。これは、正常な分子だけを選んで“適材適所”に配置するという「品質管理機構」がKCNQ2/3自身に備わっていることを示しています。
本研究成果は、てんかんを含む様々な神経・精神疾患の原因となるKCNQ2/3の機能不全が同時に、その局在異常も引き起こす可能性が高いことを示唆しており、将来的にこれら疾患の発症機序の解明や新しい治療法の開発に貢献することが期待されます。
Coupling of Functionality to Trafficking of KCNQ2/3 Potassium Channels at the Axon Initial Segment. Yoshioka D, Okamura Y. Proceedings of the National Academy of Sciences of the United States of America (PNAS) : 123(10), 2026.
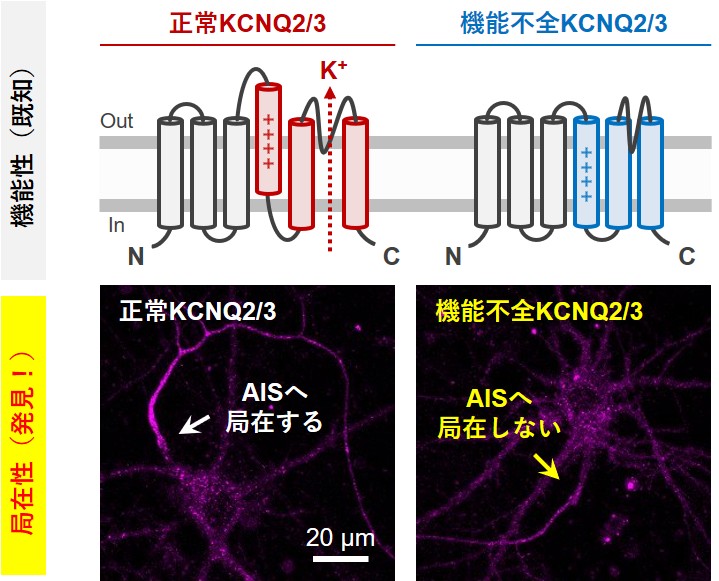
<図の説明>
図1. KCNQ2/3の機能・局在連関。正常なKCNQ2/3(左)がAISに強く局在する一方、機能不全のKCNQ2/3変異体(右)ではAIS局在効率が著しく低下することを明らかにした。矢印はAISの位置を示す。スケールバー、20 µm。